시지바이오가 환자맞춤형 임플란트를 앞세워 미국 시장에 본격 진출한다.
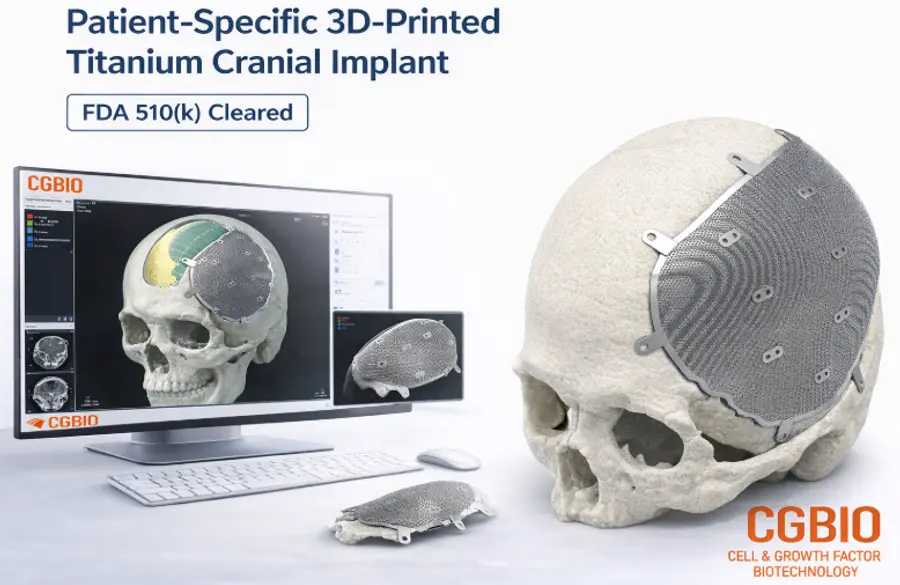
22일 시지바이오는 자사의 환자맞춤형 티타늄 임플란트 ‘이지메이드 TI(EASYMADE TI)’가 이달 9일 FDA(미 식품의약국)로 부터 510(k) 허가를 획득했다고 밝혔다.
FDA 510(k)는 기존 허가 제품과의 동등성(Substantial Equivalence)을 입증해야 하는 대표적인 시판 전 허가 절차FH, 미국 내 의료기기 판매를 위한 핵심 관문 이다.
이 허가는 국내 기업 가운데 최초로 미국 시장용 환자맞춤형 티타늄 임플란트로 허가 받은 케이스로 시지바이오의 기술력과 글로벌 인허가 대응 역량을 동시에 입증한 의미를 갖는다.
이지메이드 TI는 환자의 CT 데이터를 기반으로 설계되는 맞춤형 임플란트. 이는 두개골 및 비하중성 두개안면 결손부 재건이 주목 이다.
의료용 티타늄 합금을 사용한다. 금속 3D 프린팅 기술인 레이저 파우더 베드 융합(LPBF) 공정을 통해 제작된다.
공급 프로세스도 경쟁력이 있다. 미국 의료진이 환자의 CT 이미지를 전달하면 국내 디자인센터에서 맞춤 설계를 진행한 뒤 5일 이내 제품을 미국 병원으로 배송, 이후 병원 내 멸균 절차를 거쳐 즉시 수술에 적용할 수 있다.
이번 허가는 시지바이오의 미국 맞춤형 임플란트 사업 확대의 전환점이 될 것으로 보인다.
미국에서는 외상, 종양 절제, 감압성 두개절제술 이후 재건 수요가 꾸준히 증가하고 있다. 환자 맞춤형 재건 솔루션에 대한 관심도 높아지고 있다.
유현승 대표는 “이지메이드 TI의 FDA 510(k) 클리어런스는 환자맞춤형 재건 솔루션 분야에서 시지바이오의 글로벌 경쟁력을 입증한 성과”라고 자평하면서 “미국 시장에서 관련 사업을 본격 확대하고 후속 제품군의 글로벌 인허가와 사업화도 추진하겠다”고 말했다.
시지바이오는 이번을 계기로 미국 시장 내 사업화를 본격화하는 한편, 환자맞춤형 의료기기에서 글로벌 입지를 확대해 나기기로 했다.







