보건복지부는 2017년 우리 제약산업의 국제 경쟁력을 높이기 위해 신약을 개발한 47개 혁신형 제약기업과 현장 간담회를 갖고, 희망사항을 듣고-정보를 공유하는 시간을 가졌다.
11일 오후 보건복지부는 경기도 기흥의 종근당 효종연구소 에서 이들 혁신 제약기업과 지난해 해외기술이전, 해외시장 진출, 신제품의 출시, 국제공동연구, 국내외 투자 등의 분야에서 혁신형 제약기업이 이룩한 다양한 성과를 공유하고, 건의사항을 들었다.
복지부 에서는 양성일 보건산업정책국장 등 무려 20여명이 참석, "강력한 정책적 지원을 하겠다"는 의자를 보였다.
혁신기업 가운데는 혁신형제약기업협의회 TF팀원인 종근당, 한국오츠카, 비씨월드제약 등 8개 업체 관계자들과 제약협회, KRPIA(다국적의약산업협), 바이오의약품협회, 보건산업진흥원 등 관련단체 관계자 들도 함께했다.
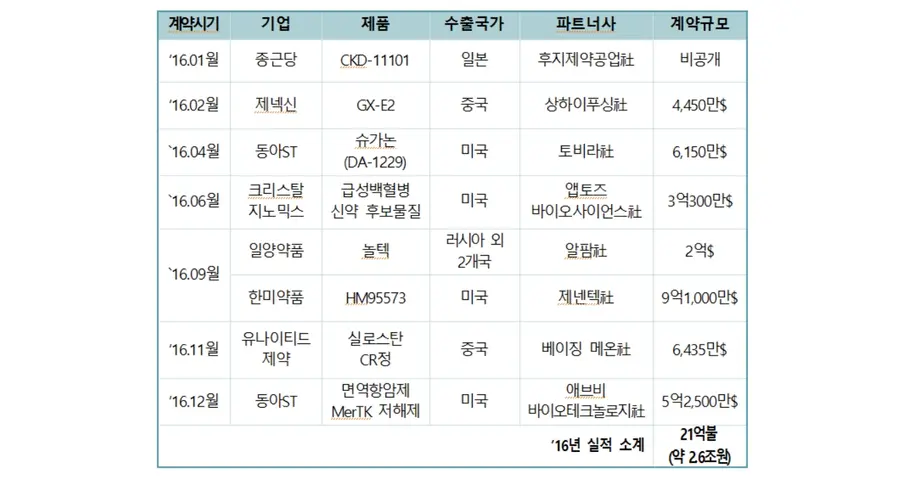
각 업체가 발표 형식으로 공개한 성과를 모아보면 ▶종근당 등 7개 기업이 일본, 중국 등에 8개의 기술을 이전, 약 2조6000억원을 벌어들였는데, 비공개 1건 등을 포함하면 2016년의 기술이전 총액은 약 3조원에 이르는 것으로 집계됐다.
업체별 성과를 보면 ▶셀트리온이 개발한 세계 최초의 항체 바이오시밀러인 류머티스관절염 치료제 〈램시마〉, ▶SK케미칼 개발 바이오신약 앱스틸라(A형 혈우병치료제)가 미국 FDA을 승인했고, 국산 제너릭의약품 가운데는 ▶대웅제약의 메로페넴주(항생제)가 최초로 FDA 승인을 받았다.
또 ▶LG생명과학이 국내선 처음으로 개발한 5가 혼합백신인 유펜타 주사(디프테리아, 파상풍, 백일해, B형간염, 뇌수막염)와 ▶녹십자는 4가 인플루엔자(독감) 백신인 지씨플루쿼드리밸런트가 세계보건기구(WHO) 사전적격심사(PQ) 승인을 획득다. ▶ 유나이티드제약은 실로스CR로 두각을 보였다.
녹십자의 사전적격심사 획득은 WHO가 백신의 품질 및 유효성·안전성 등을 심사해 국제기구 조달시장 입찰에 응찰할 수 있는 자격을 갖는다는 점에서 상당한 의미기 있다.
▶한미약품이 개발한 폐암 표적항암제 올리타정이 국내 27호 신약으로 식약처 허가를 획득했고, ▶메디톡스의 세계 최초 복합 단백질 제거 보툴리눔 톡신 A형 제제 코어톡스(Coretox), ▶셀트리온의 항암제 바이오시밀러 트룩시마, ▶보령제약의 고혈압 복합제 투베로정, ▶신풍제약의 소아용 말라리아 치료제 피라맥스과립(개량신약) 등이 시판허가를 받았다.
▶유한양행은 미국 Genosco사(오스코텍 자회사)와 비세포성 폐암의 주 재발원인 4세대 EGFR 키나제 삼중돌연변이 단백질 표적 억제 신약 공동연구 추진, ▶녹십자는 충북 오창에 혈액제제 생산시설인 PD(Plasma Derivatives) 2관을 완공, 시제품 생산에 들어갔다.
종근당 김성곤 중앙연구소장은 이 같은 성과를 올해는 한층 더 높이는데 도움이 될 수있는 글로벌 신약 연구개발 전략 등을 소개했다.
또 종근당 김 소장은 제약업계를 대표, 신약개발 R&D 지원 확대 및 세제 추가지원 등 업계의 건의사항을 발표했다.
이날 간담회에서 복지부 양성일 보건산업정책국장은 "제약산업 육성을 위해 관련 부처와 협력, 신약개발 R&D 지원의 확대, 바이오 베터·시밀러, 개량신약 등을 포함, 국내 개발 신약에 대해 약가-세제 지원 등 인센티브를 늘리는 등 적극적으로 지원할 예정"이라고 말했다.
양 국장은 "혁신형 제약기업에 대한 구체적인 지원 방안을 산학연 전문가로 구성고, 종합된 내용을, 자문단을 통해 '제2차 제약산업 육성 종합계획'에 반영, 하반기에 발표할 것"이라고 덧붙였다.







